Ein bahnbrechendes „embryoähnliches“ Modell aus Stammzellen ermöglicht Forschern erstmals die direkte Beobachtung der frühesten Phasen der menschlichen Embryonalentwicklung im Labor.
Forscher der University of Cambridge und des Hubrecht-Instituts in den Niederlanden haben dieses Modell entwickelt. Es repliziert Schlüsselmerkmale eines 20 Tage alten menschlichen Embryos, ohne jedoch das Potenzial zur Weiterentwicklung zu einem vollständigen Embryo zu besitzen.
Ihre Arbeit könnte entscheidend beitragen, die Ursachen von Geburtsfehlern, Unfruchtbarkeit und Fehlgeburten zu ergründen.
Bisher war eine direkte Untersuchung dieser Entwicklungsstadien aufgrund ethischer Restriktionen bei der Nutzung menschlicher Embryonen unmöglich.
Im Vereinigten Königreich erfordert solche Forschung eine Lizenz und unterliegt einer 14-tägigen Frist; länger als zwei Wochen nach der Befruchtung ist die Kultivierung in vitro illegal.
Das 72 Stunden alte Modell der Forscher enthält keine Gehirnzellen oder implantationsfähiges Gewebe und erfüllt somit alle geltenden ethischen Standards.
Die Studie, veröffentlicht in der renommierten Fachzeitschrift Nature, wurde von der Ethikkommission der University of Cambridge geprüft und genehmigt.
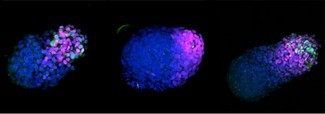
Dr. Naomi Moris, Genetikerin an der University of Cambridge und Erstautorin der Studie, erklärt: „Dieses hochinnovative Modellsystem erlaubt uns, die Prozesse der frühen menschlichen Embryonalentwicklung erstmals im Labor detailliert zu untersuchen.“
„Es markiert den ersten Schritt zur Modellierung des menschlichen Körperplans und hilft zu verstehen, was bei Fehlentwicklungen wie Geburtsfehlern schiefgeht.“
In den frühen Stadien falten sich die Zellen des Embryos zu einer dreischichtigen Struktur – ein Prozess namens Gastrulation.
Diese Schichten differenzieren sich später zu den diversen Gewebetypen des menschlichen Körpers.
Die Gastrulation setzt etwa 14 Tage nach der Befruchtung ein, weshalb Wissenschaftler diesen Mechanismus bisher nicht beobachten konnten.
Viele Geburtsfehler entstehen genau in dieser kritischen Phase.

Die Forscher analysierten die Genexpression in ihrem dreitägigen „Gastruloid“-Modell und entdeckten eine klare Signatur für die Bildung von Brustmuskeln, Knochen und Knorpel.
Obwohl Tiermodelle existieren, warnen die Experten: Medikamente wie Thalidomid wirkten bei Mäusen unbedenklich, verursachten aber schwere Geburtsfehler beim Menschen.
Daher sind präzise menschliche Modelle unerlässlich.
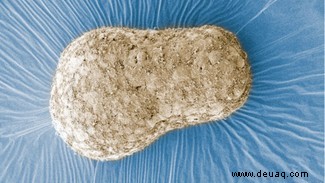
Professor Robin Lovell-Badge, Leiter des Labors für Stammzellbiologie am Francis Crick Institute, lobt das Modell als robust für diese „mysteriöse Periode“. Er fordert jedoch Validierung mit überschüssigen IVF-Embryonen – derzeit rechtlich eingeschränkt durch die 14-Tage-Regel.
„Sollte das Gesetz angepasst werden, könnten kultivierte Embryonen das Modell bestätigen. Bis dahin bleiben Zweifel an solchen Systemen bestehen.“