Wissenschaftler sind von Natur aus vorsichtig und formuliert immer Vorbehalte, selbst bei eigenen Forschungen. „Unsere Lieblingsausdrücke sind ‚Ja, aber…‘, ‚Andererseits…‘ und ‚Es bleibt unklar…‘“, erklärt Gen-Editor Dr. Fyodor Urnov. „Bitte beachten Sie das bei allem, was ich sage.”
„Falls CRISPR nur 10 Prozent unserer Visionen als Praktiker der Genbearbeitung umsetzt, wird es zu den größten Fortschritten in der Geschichte der Biomedizin gehören – mit massiven Auswirkungen auf die öffentliche Gesundheit.”
Urnov spricht per Zoom aus seinem Büro am Innovative Genomics Institute (IGI) in Berkeley, Kalifornien. Das IGI steht an der Spitze eines Durchbruchs, der das 21. Jahrhundert maßgeblich bestimmen könnte.
CRISPR ist eine Genom-Editiertechnologie, die es Forschern ermöglicht, DNA präzise zu schneiden, einzufügen oder zu löschen – um schädliche Mutationen zu korrigieren. Vereinfacht gesagt: Es erlaubt, die Bausteine des Lebens wie Text auf einem Bildschirm zu editieren. Damit können nicht nur krankheitsverursachende Gene deaktiviert werden, sondern wir entkommen auch der Genetik, mit der wir geboren wurden.
„Die Erkenntnisse sind atemberaubend – es handelt sich um beschleunigte Grundlagenforschung, die allein schon transformierend wirkt“, betont Dr. Robin Lovell-Badge vom Crick Institute. „Die Möglichkeit, genetische Erkrankungen bei Menschen zu behandeln wie nie zuvor, ist revolutionär.”
In den letzten zehn Jahren war CRISPR hauptsächlich laborbasiert. Nun verändern erste Therapien das Leben von Patienten mit schweren Erbkrankheiten. Wir stehen am Vorabend einer medizinischen Revolution, die neue Heilmittel ermöglicht – und große ethische Fragen aufwirft zu Gleichheit und Gerechtigkeit im Gesundheitswesen.
Diese Welle von Anwendungen wird mit der Industriellen Revolution oder dem Internet verglichen.

Biochemikerin Dr. Jennifer Doudna gründete das IGI als Non-Profit-Organisation, um Gen-Editing voranzutreiben, erschwinglich und zugänglich zu machen. Angesichts des enormen Potenzials gewährte das IGI-Team BBC Science Focus exklusive Einblicke.
Auf dem Berkeley-Campus entwickelten Doudna und Dr. Emmanuelle Charpentier vor fast einem Jahrzehnt CRISPR-Cas9 – das Tool, das 2020 mit dem Nobelpreis gekrönt wurde.
„Wir spürten beide ein Kribbeln, als wüáde etwas Großes entstehen“, erinnert sich Doudna. „Keiner ahnte damals, wohin das führen würde.”
CRISPR ist vielseitiger, einfacher und günstiger als Alternativen. Sein Tempo ist beispiellos: Von der Entdeckung zu Humanstudien in unter einem Jahrzehnt.
„Es ist wie ein Schleudertrauma“, vergleicht IGI-Geschäftsführer Dr. Brad Ringeisen. „Nanopartikel brauchten 30–40 Jahre bis zum COVID-Impfstoff.”
Erste CRISPR-Erfolge
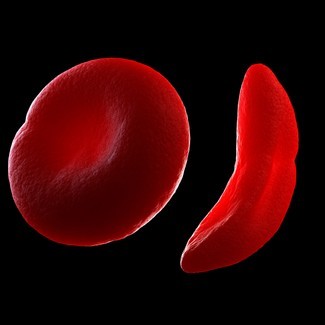
Patienten mit Sichelzellenanämie profitieren als Erste. 2019 erhielt Victoria Gray als eine der ersten eine CRISPR-Therapie.
Sie litt unter Schmerzen, Transfusionen und Risiken wie Schlaganfall durch mutierte rote Blutkörperchen.
Die Therapie: Knochenmarkzellen extrahiert, CRISPR aktiviert fötales Hämoglobin, Chemotherapie, Reinfusion. Gray braucht nun keine Medikamente mehr – sie ist geheilt.

„Sichelzellenanämie ist ein ideales Ziel: Ein Gen editieren, um Symptome zu lindern“, sagt Ringeisen. „Betroffen sind 100.000 in den USA, über eine Million weltweit.”
Das IGI forscht zu Blut-, Autoimmun-, Neurologie-, Krebs- und COVID-Erkrankungen. Fokus: CRISPR-T-Zellen als Immuntruppen.
Dr. Alex Marson, IGI-Direktor für menschliche Gesundheit, testet korrigierte T-Zellen bei Autoimmunfamilien.
„Wir haben Labortests; nun kommt die klinische Studie.” Er visioniert skalierbare, günstige T-Zelltherapien.
„Wir können Infektionen bekämpfen, indem wir DNA-Sprache in Immunzellen schreiben.”
CRISPR wirkt bei allen genetisch beeinflussten Krankheiten: Krebs, Herzkrankheiten, Neurodegeneration, Arthritis.
„Alle Krankheiten sind im Visier“, fasst Ringeisen zusammen.
Krankheiten vorbeugen
Gen-Editing schützt durch schützende Varianten oder Korrekturen.
„Seltene Individuen mit schützenden Mutationen senken Herzrisiken drastisch“, erklärt Urnov.
Doudna sieht CRISPR präventiv: „Genom sequenzieren, Risikogene editieren – vor der Krankheit.”
Wie bei Ernährung oder Mastektomie: Würden Sie Ihre DNA editieren?
Verschwörungstheorien und GMO-Skepsis bremsen Akzeptanz.
„Missverständnisse können Fortschritte behindern“, warnt Doudna.
2018: CRISPR-Babys in China. Dr. He Jiankui editierte Embryonen für HIV-Schutz – ethisch verurteilt, inhaftiert.

Er veränderte die Keimbahn unsicher. Kritik: Off-Target-Effekte, Krebsrisiko.
„Ein schwerwiegendes Ereignis, das das Feld beschädigt“, sagt Urnov. Fokus auf 250 Millionen mit genetischen Krankheiten, nicht Designerbabys.
Delivery-Challenge: Präzise Lieferung. IGI-Forscher wie Dr. Ross Wilson testen methodisch.

„Sicherheit durch Studien beweisen.” CRISPRoff editiert Epigenom ohne DNA-Schnitt.
„Risiko-Nutzen-Balance ist vielversprechend“, betont Wilson.
Risiko einer genetischen Kluft?
Doudna will CRISPR zum Standard machen – Kosten sind Schlüssel.
Ohne Zugang für Alle entsteht Ungleichheit. IGI priorisiert Skalierbarkeit und Gerechtigkeit.
„Therapien kosten Millionen; Europa zögert“, kritisiert Urnov.
Seltene Mutationen fehlen kommerziellem Interesse.
„Von Anfang an kostengerecht denken“, fordert Lovell-Badge.
IGI baut skalierbare Pipelines für Entdeckung bis Markteinführung.
„Technologie für alle – das ist unsere Mission“, betont Doudna.
Die Revolution kommt. Doudna sorgt dafür, dass sie inklusiv ist.
- Dieser Artikel erschien zuerst in Ausgabe 367 des BBC Science Focus Magazine.