Stellen Sie sich ein kaltes Getränk an einem heißen Tag vor – ohne schwebende Eiswürfel würde es deutlich weniger ansprechend wirken. Aber warum schwimmt Eis auf Wasser? Und was bestimmt überhaupt, ob etwas schwimmt?
Das Archimedes-Prinzip: Der Schlüssel zum Schwimmen
Ein Objekt schwimmt, wenn seine Dichte geringer ist als die des Wassers. Dieses Prinzip erklärt das Archimedes-Prinzip, benannt nach dem griechischen Mathematiker, der es in seiner Badewanne entdeckte.
Vorab eine Warnung: Die Erklärung enthält etwas Mathematik, die wir aber klar und praxisnah darstellen.
Wenn Sie ein Objekt ins Wasser tauchen, entsteht eine Auftriebskraft (F), die gegen die Schwerkraft wirkt. Sie entspricht dem Gewicht des verdrängten Wassers. Das Gewicht ist Masse mal Erdbeschleunigung (g). Also: F = Dichte des Wassers × Volumen des verdrängten Wassers × g.
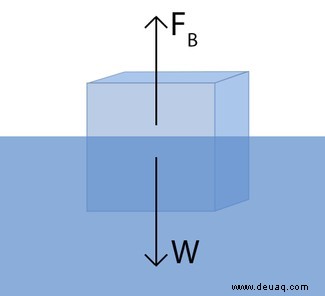
Archimedes' Erkenntnis: Das verdrängte Volumen entspricht dem Volumen des untergetauchten Objekts. Die Auftriebskraft F ist also Dichte_Wasser × Volumen_Objekt × g. Sie gleicht die Schwerkraft (Gewicht des Objekts = Dichte_Objekt × Volumen_Objekt × g) aus, wenn Dichte_Objekt < Dichte_Wasser.
Zusammengefasst: Objekte schwimmen, wenn sie weniger dicht als Wasser sind.
Warum sind Feststoffe meist dichter als Flüssigkeiten?
Feststoffe sind normalerweise dichter als ihre Flüssigformen, da Moleküle im Festkörper eng im Kristallgitter gepackt sind.

Beim Erhitzen schwingen Moleküle stärker, lösen sich schließlich und bilden eine Flüssigkeit – mit größerem Volumen und geringerer Dichte. Weiteres Erhitzen erzeugt Gas mit noch niedrigerer Dichte.

Bei Phasenwechseln nimmt die Dichte ab – eine allgemeine Regel.
Warum ist Eis die Ausnahme? Die Rolle der Wasserstoffbrückenbindungen
Wasser ist ein Sonderfall dank Wasserstoffbrückenbindungen. Ein Wassermolekül (H₂O) ist V-förmig: Sauerstoff in der Mitte, zwei Wasserstoffatome. Kovalente Bindungen halten es zusammen, doch Sauerstoff zieht Elektronen stärker an – das Molekül ist polar.
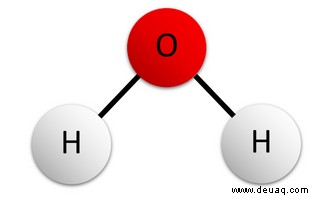
Gegensätzliche Ladungen bilden Wasserstoffbrückenbindungen zwischen Molekülen. In der Flüssigkeit brechen und bilden sie ständig neu. Beim Gefrieren ordnen sich Moleküle im Kristallgitter: Abstoßung gleicher Ladungen schafft mehr Abstand – Eis ist ca. 9 % weniger dicht als flüssiges Wasser.
Kann man die Ausdehnung von Eis verhindern?
Wasser ist bei 4 °C am dichtesten. Beim Abkühlen dehnt es sich aus. Gefrorenes Wasser erhöht sein Volumen um 9 %. Der Druck beträgt bis zu 790 Megapascal (7.800 Atmosphären). Professor Martin Chaplin von der London South Bank University, weltweit führender Experte für Wassereigenschaften, bestätigt: Kein irdisches Material hält das stand. – Robert Matthews
Gefriert Wasser unter hohem Druck anders?
In einem starren Behälter steigt der Druck bei Gefrieren rapide. Ab ca. 200 Megapascal (2.000 Atmosphären) bilden sich kompaktere Eismodifikationen wie Eis III neben Eis Ih. Es gibt 13 Eisformen. – Keiron Allen